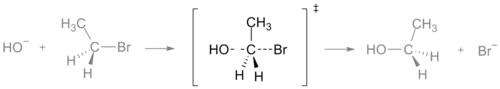Bir kimyasal reaksiyonda geçiş durumu, maksimum enerji değerinin olduğu noktadır. Bu enerjiye aktivasyon enerjisi denir. İki veya daha fazla molekül karıştırıldığında birbirlerine çarpacaklardır. Geçiş durumundan geçmek için yeterli enerjiyle çarpışırlarsa, reaksiyona girecek ve yeni moleküller oluşturacaklardır. Geçiş durumunda, eski bağlar koparken yeni bağlar oluşur. Bir grafikte veya çizimde, geçiş durumu genellikle çift hançer ‡ sembolü ile işaretlenir.
Bir geçiş durumunu incelemek çok zordur. Bunun nedeni, enerjinin çok yüksek olması ve moleküllerin çok kısa bir süre, genellikle femtosaniyeler boyunca bu formda kalmasıdır. Geçiş durumlarını ara ürünlerle karıştırmamak önemlidir. Ara haller minimum enerji noktalarında bulunur ve çok uzun süre yaşayabilirler. Bununla birlikte, bir geçiş hali gibi, bir ara ürün de bir reaksiyonun reaktifleri ve ürünleri arasındadır.
Reaksiyon mekanizmalarını anlamak için geçiş durumlarını incelemek çok önemlidir. Geçiş durumunun nasıl göründüğünü hesaplamak için kullanılabilecek teoriler ve bilgisayar programları vardır. Bu, kimyasal kinetiğin bir parçasıdır.