Sentez
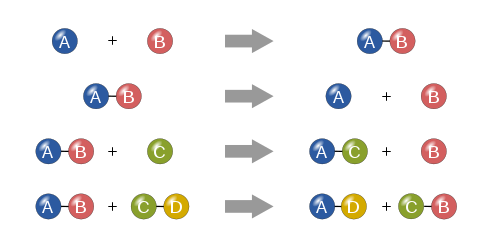
Bir sentez reaksiyonunda, iki veya daha fazla basit madde birleşerek daha karmaşık bir madde oluşturur.
A + B ⟶ A B {\displaystyle A+B\longrightarrow AB} 
"Bir ürün veren iki veya daha fazla reaktan" bir sentez reaksiyonunu tanımlamanın başka bir yoludur. Bir sentez reaksiyonu örneği, demir ve sülfürün demir (II) sülfür oluşturmak üzere birleşmesidir:
8 F e + S 8 ⟶ 8 F e S {\displaystyle 8Fe+S_{8}\longrightarrow 8FeS} 
Bir başka örnek de basit hidrojen gazının basit oksijen gazı ile birleşerek su gibi daha karmaşık bir madde üretmesidir.
Ayrıştırma
Ayrışma reaksiyonu, daha karmaşık bir maddenin daha basit parçalarına ayrılmasıdır. Bu nedenle sentez reaksiyonunun tersidir ve şu şekilde yazılabilir:
A B ⟶ A + B {\displaystyle AB\longrightarrow A+B} 
Bir ayrışma reaksiyonu örneği, oksijen ve hidrojen gazı yapmak için suyun elektrolizidir:
2 H 2 O ⟶ 2 H 2 + O 2 {\displaystyle 2H_{2}O\longrightarrow 2H_{2}+O_{2}} 
Tekli değiştirme
Tekli yer değiştirme reaksiyonunda, birleşik olmayan tek bir element bir bileşikteki başka bir elementin yerini alır; başka bir deyişle, bir element bir bileşikteki başka bir elementle yer değiştirir Bu reaksiyonlar genel olarak şu şekildedir:
A + B C ⟶ A C + B {\displaystyle A+BC\longrightarrow AC+B} 
Tek bir yer değiştirme reaksiyonuna örnek olarak magnezyumun suda hidrojenle yer değiştirerek magnezyum hidroksit ve hidrojen gazı oluşturması verilebilir:
M g + 2 H 2 O ⟶ M g ( O H ) 2 + H 2 {\displaystyle Mg+2H_{2}O\longrightarrow Mg(OH)_{2}+H_{2}} 
Çift değiştirme
Çift yer değiştirme reaksiyonunda, iki bileşiğin anyon ve katyonları yer değiştirir ve tamamen farklı iki bileşik oluşturur. Bu reaksiyonlar genel formdadır:
A B + C D ⟶ A D + C B {\displaystyle AB+CD\longrightarrow AD+CB} 
Örneğin, baryum klorür (BaCl2 ) ve magnezyum sülfat (MgSO4 ) reaksiyona girdiğinde, SO42− anyonu 2Cl− anyonu ile yer değiştirerek BaSO4 ve MgCl2 bileşiklerini verir.
Çift yer değiştirme reaksiyonuna bir başka örnek de kurşun(II) nitratın potasyum iyodür ile reaksiyona girerek kurşun(II) iyodür ve potasyum nitrat oluşturmasıdır:
P b ( N O 3 ) 2 + 2 K I ⟶ P b I 2 + 2 K N O 3 {\displaystyle Pb(NO_{3})_{2}+2KI\longrightarrow PbI_{2}+2KNO_{3}}