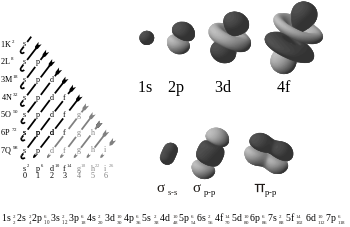
Kimyada pi bağları (π bağları), bir elektronun yörünge yolunun diğerinin yörünge yolu ile kesiştiği (örtüştüğü) kovalent kimyasal bağlardır. Elektronlar lob şeklinde bir sekiz yoluna sahiptir (resme bakınız). Yollar her iki lobda da çakıştığı için iki çakışma alanı vardır. Yörüngenin düğüm düzlemlerinden yalnızca biri ilgili çekirdeklerin her ikisinden de geçer.
İsimlerindeki Yunanca π harfi p orbitallerini ifade eder. Pi bağının orbital simetrisi, bağ ekseninden bakıldığında p orbitali ile aynı görünür. P orbitalleri genellikle bu tür bir bağa sahiptir. D orbitallerinin de pi bağı kullandığı varsayılır ancak gerçekte böyle olması gerekmez. D orbitallerinin bağlanması fikri hipervalans teorisine uymaktadır.
Pi bağları genellikle sigma bağlarından daha zayıftır. Kuantum mekaniğine göre bunun nedeni yörünge yollarının paralel olması ve böylece p-yörüngeleri arasında çok daha az örtüşme olmasıdır.
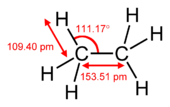
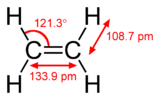
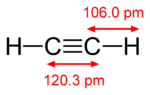
Pi bağları, iki atomik orbital iki örtüşme alanı aracılığıyla temas halinde olduğunda meydana gelir. Pi bağları sigma bağlarına göre daha yayılmış bağlardır. Pi bağlarındaki elektronlar bazen pi elektronları olarak adlandırılır. Bir pi bağı ile birleşen moleküler parçalar, pi bağını kırmadan bu bağ etrafında dönemezler. Dönme, iki p orbitalinin paralel yollarını yok eder.