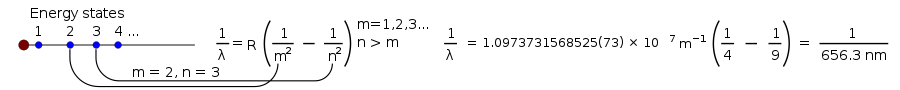Kuantum mekaniği formülleri ve fikirleri, parlayan hidrojenden gelen ışığı açıklamak için yapılmıştır. Atomun kuantum teorisi, diğer fikirlerin açıklayamadığı elektronun neden yörüngesinde kaldığını da açıklamak zorundaydı. Eski fikirlere göre elektron atomun merkezine düşmek zorundaydı çünkü başlangıçta kendi enerjisi tarafından yörüngede tutuluyordu, ancak yörüngesinde dönerken enerjisini hızla kaybediyordu. (Çünkü elektronların ve diğer yüklü parçacıkların ışık yaydıkları ve hız değiştirdiklerinde ya da döndüklerinde enerji kaybettikleri biliniyordu).
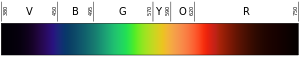
Hidrojen lambaları neon ışıkları gibi çalışır, ancak neon ışıklarının kendine özgü bir ışık rengi (ve frekansı) grubu vardır. Bilim insanları, tüm elementleri ürettikleri ışık renklerine göre tanımlayabileceklerini öğrendiler. Sadece frekansların nasıl belirlendiğini çözemediler.
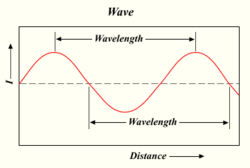
Daha sonra Johann Balmer adında İsviçreli bir matematikçi, λ'nın (dalga uzunluğu için lambda) ne olacağını söyleyen bir denklem buldu:
λ = B ( n 2 n 2 - 4 ) n = 3 , 4 , 5 , 6 {\displaystyle \lambda =B\left({\frac {n^{2}}{n^{2}-4}}\right)\qquad \qquad n=3,4,5,6} 
Burada B, Balmer'in 364,56 nm'ye eşit olarak belirlediği bir sayıdır.
Bu denklem sadece bir hidrojen lambasından gelen görünür ışık için işe yarıyordu. Ancak daha sonra denklem daha genel hale getirildi:
1 λ = R ( 1 m 2 - 1 n 2 ) , {\displaystyle {\frac {1}{\lambda }}=R\left({\frac {1}{m^{2}}-{\frac {1}{n^{2}}}\right),} 
Burada R, 0,0110 nm'ye eşit olan Rydberg sabitidir−1 ve n, m'den büyük olmalıdır.
m ve n için farklı sayılar koyarak, birçok ışık türü (ultraviyole, görünür ve kızılötesi) için frekansları tahmin etmek kolaydır. Bunun nasıl çalıştığını görmek için Hyperphysics'e gidin ve sayfanın ortasından aşağıya inin. (Hidrojen için H = 1 kullanın.)
1908 yılında Walter Ritz, frekanslar arasındaki belirli boşlukların kendilerini nasıl tekrarladığını gösteren Ritz kombinasyon prensibini ortaya koymuştur. Bunun birkaç yıl sonra Werner Heisenberg için önemli olduğu ortaya çıktı.
1905 yılında Albert Einstein, Planck'ın fikrini kullanarak bir ışık demetinin foton adı verilen parçacıklardan oluştuğunu gösterdi. Her fotonun enerjisi frekansına bağlıdır. Einstein'ın fikri, kuantum mekaniğinde elektronlar, protonlar, nötronlar ve diğerleri gibi tüm atom altı parçacıkların aynı anda hem dalga hem de parçacık olduğu fikrinin başlangıcıdır. (Atomda elektronun dalga olarak bulunduğu atom resmine bakınız.) Bu, atom altı parçacıklar ve elektromanyetik dalgalar hakkında dalga-parçacık ikiliği adı verilen bir teoriye yol açmıştır. Bu, parçacıkların ve dalgaların ne biri ne de diğeri olduğu, ancak her ikisinin de belirli özelliklerine sahip olduğu yerdir.
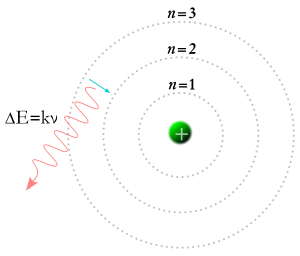
1913 yılında Niels Bohr, elektronların bir atomun çekirdeği etrafında yalnızca belirli yörüngelerde yer alabileceği fikrini ortaya attı. Bohr'un teorisine göre, yukarıdaki denklemde m ve n olarak adlandırılan sayılar yörüngeleri temsil edebilir. Bohr'un teorisine göre elektronlar m yörüngesinde başlayıp n yörüngesinde sonlanabilir ya da bir elektron n yörüngesinde başlayıp m yörüngesinde sonlanabilir, dolayısıyla bir foton bir elektrona çarparsa enerjisi emilir ve elektron bu ekstra enerji nedeniyle daha yüksek bir yörüngeye hareket eder. Bohr'un teorisine göre, eğer bir elektron daha yüksek bir yörüngeden daha düşük bir yörüngeye düşerse, o zaman bir foton şeklinde enerji vermek zorunda kalacaktır. Fotonun enerjisi iki yörünge arasındaki enerji farkına eşit olacaktır ve bir fotonun enerjisi onun belirli bir frekansa ve renge sahip olmasını sağlar. Bohr'un teorisi atom altı olayların birçok yönüne iyi bir açıklama getirmiş, ancak parlayan hidrojen (ve parlayan neon veya başka herhangi bir element) tarafından üretilen ışık renklerinin her birinin neden kendine özgü bir parlaklığa sahip olduğunu ve parlaklık farklarının her element için her zaman aynı olduğunu yanıtlayamamıştır.
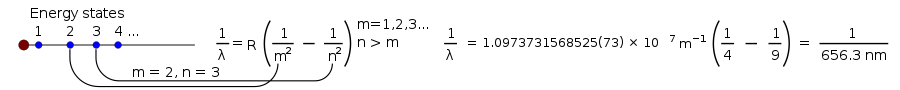
Niels Bohr teorisini ortaya attığında, bir hidrojen lambasının ürettiği ışıkla ilgili çoğu şey biliniyordu, ancak bilim adamları hala parlayan hidrojen tarafından üretilen çizgilerin her birinin parlaklığını açıklayamıyorlardı.
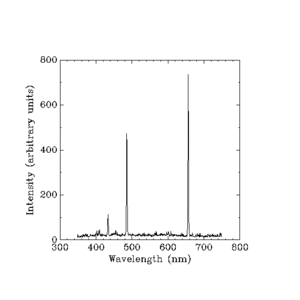
Werner Heisenberg her bir çizginin parlaklığını ya da "yoğunluğunu" açıklama işini üstlendi. Balmer'in bulduğu gibi basit bir kural kullanamadı. Her şeyi bir elektronun kütlesi (ağırlığı), bir elektronun yükü (statik elektrik gücü) ve diğer küçük miktarlar gibi şeyler açısından hesaplayan klasik fiziğin çok zor matematiğini kullanmak zorunda kaldı. Klasik fiziğin bir hidrojen lambasının ürettiği renk bantlarının parlaklığı için zaten cevapları vardı, ancak klasik teori dört ayrı renk bandı değil, sürekli bir gökkuşağı olması gerektiğini söylüyordu. Heisenberg'in açıklaması şöyledir:
Parlayan hidrojenin hangi frekanslarda ışık üreteceğini söyleyen bir yasa vardır. İlgili elektronlar atomun çekirdeğine (merkezine) yakın yörüngeler arasında hareket ederken aralıklı frekansları tahmin etmek zorundadır, ancak aynı zamanda elektronun daha uzak yörüngeler arasında hareket ederken ne yaptığına baktığımızda frekansların birbirine daha da yaklaşacağını tahmin etmek zorundadır. Ayrıca, dışarı çıktıkça frekanslar arasındaki yoğunluk farklarının birbirine daha da yaklaşacağını tahmin edecektir. Klasik fiziğin zaten tek bir denklem setiyle doğru cevapları verdiği yerde, yeni fizik aynı cevapları farklı denklemlerle vermek zorundadır.
Klasik fizik, fiziksel dünyanın matematiksel bir resmini yapmak için Fransız matematikçi Fourier'in yöntemlerini kullanır ve bu durumda, bazı ışıklardan gelen tüm frekanslardaki ışık yoğunluklarını veren tek bir düzgün eğri yapmak için bir araya gelen düzgün eğri koleksiyonlarını kullanır. Ancak bu doğru değildir çünkü bu düzgün eğri sadece yüksek frekanslarda ortaya çıkar. Daha düşük frekanslarda her zaman izole noktalar vardır ve hiçbir şey noktaları birbirine bağlamaz. Dolayısıyla, gerçek dünyanın bir haritasını çıkarmak için Heisenberg büyük bir değişiklik yapmak zorunda kaldı. Sadece doğada görülenlerle eşleşecek sayıları seçmek için bir şeyler yapması gerekiyordu. Bazen insanlar onun bu denklemleri "tahmin ettiğini" söyler, ancak o körü körüne tahminler yapmıyordu. İhtiyacı olanı buldu. Hesapladığı sayılar bir grafik üzerinde noktalar oluşturacaktı, ancak noktalar arasında bir çizgi olmayacaktı. Ve her hesaplama kümesi için sadece noktalardan oluşan bir "grafik" yapmak çok fazla kağıt israfına neden olur ve hiçbir şey yapılmasını sağlamazdı. Heisenberg, farklı frekanslar için yoğunlukları verimli bir şekilde tahmin etmenin ve bu bilgileri yararlı bir şekilde düzenlemenin bir yolunu buldu.
Balmer'in başlattığı ve Rydberg'in geliştirdiği yukarıda verilen deneysel kuralı kullanarak, Heisenberg'in istediği türden bir resim elde etmesine yardımcı olacak bir dizi sayının nasıl elde edileceğini görebiliriz:
Bu kurala göre elektron bir yörüngeden diğerine hareket ettiğinde, merkezden uzaklaşmasına ya da merkeze yaklaşmasına bağlı olarak enerji kazanır ya da kaybeder. Böylece bu yörüngeleri ya da enerji seviyelerini bir ızgaranın üst ve yan kısımlarına başlıklar halinde yerleştirebiliriz. Tarihsel nedenlerden dolayı en düşük yörüngeye n denir ve bir sonraki yörüngeye n - a denir, sonra n - b gelir ve bu böyle devam eder. Elektronlar aslında enerji kazanırken negatif sayılar kullanmaları kafa karıştırıcıdır, ancak bu böyledir.
Rydberg kuralı bize frekansları verdiğinden, elektronun nereye gittiğine bağlı olarak sayıları koymak için bu kuralı kullanabiliriz. Eğer elektron n'de başlayıp n'de bitiyorsa, o zaman gerçekten hiçbir yere gitmemiştir, yani enerji kazanmamış ve enerji kaybetmemiştir. Eğer elektron n-a'da başlayıp n'de bitiyorsa, o zaman daha yüksek bir yörüngeden daha düşük bir yörüngeye düşmüştür. Eğer bunu yaparsa enerji kaybeder ve kaybettiği enerji foton olarak ortaya çıkar. Fotonun belirli bir miktarda enerjisi vardır, e, ve bu e = h f denklemiyle belirli bir f frekansıyla ilişkilidir. Bu yüzden belirli bir yörünge değişikliğinin belirli bir ışık frekansı üreteceğini biliyoruz, f. Eğer elektron n'de başlar ve n - a'da biterse, bu daha düşük bir yörüngeden daha yüksek bir yörüngeye gittiği anlamına gelir. Bu sadece dışarıdan belirli bir frekansta ve enerjide bir foton geldiğinde, elektron tarafından emildiğinde ve ona enerjisini verdiğinde gerçekleşir ve elektronun daha yüksek bir yörüngeye çıkmasını sağlayan şey budur. Bu yüzden, her şeyi anlamlı kılmak için, bu frekansı negatif bir sayı olarak yazıyoruz. Belli bir frekansa sahip bir foton vardı ve şimdi o foton yok oldu.
Böylece şöyle bir tablo oluşturabiliriz; burada f(a←b), bir elektron b enerji durumundan (yörüngesinden) a enerji durumuna geçtiğinde oluşan frekansı ifade eder (Yine, diziler ters görünüyor, ancak orijinal olarak bu şekilde yazılmışlardır):
F ızgara
| Elektron Durumları | n | n-a | n-b | n-c | .... | |
| n | f(n←n) | f(n←n-a) | f(n←n-b) | f(n←n-c) | ..... | |
| n-a | f(n-a←n) | f(n-a←n-a) | f(n-a←n-b) | f(n-a←n-c) | ..... | |
| n-b | f(n-b←n) | f(n-b←n-a) | f(n-b←n-b) | f(n-b←n-c) | ..... | |
| geçiş.... | ..... | ..... | ..... | ..... | | |
Heisenberg ızgaraları bu şekilde yapmadı. Sadece aradığı yoğunlukları elde etmesini sağlayacak matematiği yaptı. Ancak bunu yapmak için iki genliği (bir dalganın ne kadar yüksek ölçtüğünü) çarparak yoğunluğu hesaplaması gerekiyordu. (Klasik fizikte yoğunluk, genliğin karesine eşittir.) Bu sorunu çözmek için garip görünümlü bir denklem oluşturdu, makalesinin geri kalanını yazdı, patronuna verdi ve tatile çıktı. Dr. Born onun komik denklemine baktı ve biraz çılgınca göründü. "Heisenberg bana bu garip şeyi neden verdi?" diye merak etmiş olmalı. Neden bu şekilde yapmak zorunda?" Sonra zaten çok iyi bildiği bir şeyin planına baktığını fark etti. Örneğin frekanslar için tüm matematiği yaparak yazabildiğimiz ızgara ya da tabloya matris demeye alışkındı. Heisenberg'in tuhaf denklemi de ikisini çarpmanın bir kuralıydı. Max Born çok ama çok iyi bir matematikçiydi. Çarpılan iki matris (ızgara) farklı şeyleri temsil ettiğinden (örneğin konum (x,y,z) ve momentum (mv) gibi), ilk matrisi ikinciyle çarptığınızda bir yanıt, ikinci matrisi ilk matrisle çarptığınızda başka bir yanıt elde edeceğinizi biliyordu. Matris matematiğini bilmemesine rağmen, Heisenberg bu "farklı cevaplar" problemini zaten görmüştü ve bu onu rahatsız etmişti. Ancak Dr. Born o kadar iyi bir matematikçiydi ki, ilk matris çarpımı ile ikinci matris çarpımı arasındaki farkın her zaman Planck sabiti h'nin negatif birin karekökü i ile çarpımını içereceğini gördü. Böylece Heisenberg'in keşfinden sonraki birkaç gün içinde, Heisenberg'in "belirsizlik ilkesi" olarak adlandırmaktan hoşlandığı şeyin temel matematiğine sahip oldular. Heisenberg "belirsiz" derken, elektron gibi bir şeyin sabitlenene kadar sabitlenemeyeceğini kastediyordu. Bu biraz da sürekli etrafta ezilen ve siz onu öldürmedikçe "tek bir yerde" kalamayan bir denizanasına benzer. Daha sonra insanlar bunu "Heisenberg'in belirsizlik ilkesi" olarak adlandırmayı alışkanlık haline getirdiler ve bu da birçok insanın elektronların ve benzeri şeylerin gerçekten "bir yerde" olduğunu ama bizim sadece kendi zihnimizde bu konuda belirsiz olduğumuzu düşünme hatasına düşmesine neden oldu. Bu düşünce yanlıştır. Heisenberg'in bahsettiği şey bu değildi. Bir şeyi ölçmekte zorlanmak bir sorundur, ancak Heisenberg'in bahsettiği sorun bu değildir.
Heisenberg'in fikrini kavramak çok zordur, ancak bir örnekle daha açık hale getirebiliriz. Öncelikle, bu ızgaraları "matris" olarak adlandırmaya başlayacağız, çünkü yakında matris çarpımı hakkında konuşmamız gerekecek.
Konum (q) ve momentum (p) olmak üzere iki tür ölçümle başladığımızı varsayalım. 1925 yılında Heisenberg buna benzer bir denklem yazdı:
Y ( n , n - b ) = ∑ a p ( n , n - a ) q ( n - a , n - b ) {\displaystyle Y(n,n-b)=\sum _{a}^{}\,p(n,n-a)q(n-a,n-b)} (Eşlenik değişkenler momentum ve konum için denklem)
(Eşlenik değişkenler momentum ve konum için denklem)
O bunu bilmiyordu, ama bu denklem iki matris (ızgara) yazmak ve bunları çarpmak için bir plan veriyor. Bir matrisi diğeriyle çarpmanın kuralları biraz karışıktır, ancak işte plana göre iki matris ve ardından bunların çarpımı:
P matrisi
| Elektron Durumları | n-a | n-b | n-c | .... | |
| n | p(n←n-a) | p(n←n-b) | p(n←n-c) | ..... | |
| n-a | p(n-a←n-a) | p(n-a←n-b) | p(n-a←n-c) | ..... | |
| n-b | p(n-b←n-a) | p(n-b←n-b) | p(n-b←n-c) | ..... | |
| geçiş.... | ..... | ..... | ..... | ..... | |
q matrisi
| Elektron Durumları | n-b | n-c | n-d | .... | |
| n-a | q(n-a←n-b) | q(n-a←n-c) | q(n-a←n-d) | ..... | |
| n-b | q(n-b←n-b) | q(n-b←n-c) | q(n-b←n-d) | ..... | |
| n-c | q(n-c←n-b) | q(n-c←n-c) | q(n-c←n-d) | ..... | |
| geçiş.... | ..... | ..... | ..... | ..... | |
Heisenberg'in 1925 tarihli makalesindeki ilgili denklemde belirtildiği gibi yukarıdaki iki matrisin çarpımı için matris şöyledir:
| Elektron Durumları | n-b | n-c | n-d | ..... |
| n | A | ..... | ..... | ..... |
| n-a | ..... | B | ..... | ..... |
| n-b | ..... | ..... | C | ..... |
Nerede?
A=p(n←n-a)*q(n-a←n-b)+p(n←n-b)*q(n-b←n-b)+p(n←n-c)*q(n-c←n-b)+.....
B=p(n-a←n-a)*q(n-a←n-c)+p(n-a←n-b)*q(n-b←n-c)+p(n-a←n-c)*q(n-c←n-c)+.....
C=p(n-b←n-a)*q(n-a←n-d)+p(n-b←n-b)*q(n-b←n-d)+p(n-b←n-c)*q(n-d←n-d)+.....
ve benzeri.
Matrisler ters çevrilirse, aşağıdaki değerler ortaya çıkacaktır:
A=q(n←n-a)*p(n-a←n-b)+q(n←n-b)*p(n-b←n-b)+q(n←n-c)*p(n-c←n-b)+.....
B=q(n-a←n-a)*p(n-a←n-c)+q(n-a←n-b)*p(n-b←n-c)+q(n-a←n-c)*p(n-c←n-c)+.....
C=q(n-b←n-a)*p(n-a←n-d)+q(n-b←n-b)*p(n-b←n-d)+q(n-b←n-c)*p(n-d←n-d)+.....
ve benzeri.
Çarpma işleminin sırasını değiştirmenin gerçekte çarpılan sayıları adım adım nasıl değiştirdiğine dikkat edin.