Kovalent bağlar, metal olmayan iki atom arasındaki kimyasal bağlardır. Hidrojen (H) ve oksijenin (O) birbirine bağlanarak (H2 O) oluşturduğu su buna bir örnektir. Tam bir dış kabuk genellikle sekiz elektrona ya da hidrojen veya helyum durumunda iki elektrona sahiptir. Değerlik elektronları, atomun dış kabuğunda nispeten gevşek olarak tutulan elektronlardır. Elektron kabuklarının yapısı kuantum mekaniği tarafından belirlenir).
Bir atomdaki elektronların sayısı, atomdaki protonların sayısına göre belirlenir. Elektronlar atom çekirdeğinin yörüngesinde dolanır ve atom çekirdeğinin etrafındaki bulanık yörüngeler gibidirler. İlk katmanda en fazla iki elektron bulunur. Bundan sonraki katmanlar genellikle sekize kadar elektron içerir. Kovalent bağlar, atomların değerlik elektronlarını paylaşmasıyla oluşur.
Örneğin bir atomun dokuz elektronu varsa, ilk ikisi çekirdeğe çok yakın, sonraki yedisi ise biraz daha uzakta yörüngede dolanır. Dıştaki yedi elektron, pozitif yüklü çekirdekten daha uzakta oldukları için içteki iki elektrona göre daha az sıkı tutulurlar. Bu atom, dış kabuğunda gevşek tutulan bir elektrona sahip başka bir atoma yaklaşırsa, gevşek tutulan elektron için yeni bir yörünge kullanılabilir hale gelecektir. Bu yeni elektron orbitali her iki atom çekirdeğine de bağlıdır ve orijinal elektron orbitalinden daha düşük bir enerji seviyesine sahiptir. Elektron kendiliğinden buna atlayabilir ve fazla enerjiyle bir foton yayabilir. Artık her iki atomun da yörüngesinde bir elektron vardır ve bu da elektronu sağlayan atomun küçük bir net pozitif yüke ve diğer atomun da küçük bir net negatif yüke sahip olmasıyla sonuçlanır. İki atom artık pozitif ve negatif yükler arasındaki elektromanyetik çekim kuvveti tarafından bir arada tutulmaktadır. Buna kovalent bağ denir. Bu bağı kırmak için, bağ oluşurken açığa çıkan enerji kadar enerji gerekir.
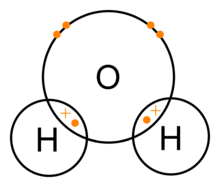
Bir su molekülü, kovalent bir bağ ile bir arada tutulan bir oksijen atomu ve iki hidrojen atomundan oluşur. Bu durumda oksijen atomu her hidrojen atomu ile bir elektron paylaşır. Bu, oksijen atomlarının küçük bir net pozitif yüke ve hidrojen atomunun küçük bir net negatif yüke sahip olduğu anlamına gelir. Sonuç olarak, oksijen ve hidrojen atomları elektromanyetik kuvvet nedeniyle birbirlerini çekerler. Bu nedenle su molekülü polar bir moleküldür: yükü eşit olarak dağılmamıştır.