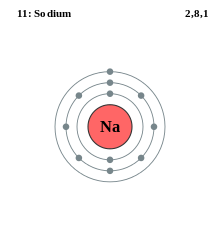
Bir elektron kabuğu, atom çekirdeğinin etrafındaki bir atomun dış kısmıdır. Elektronların bulunduğu yerdir ve temel kuantum sayısı n'nin aynı değerine sahip bir grup atomik orbitaldir.
Elektron kabuklarının bir veya daha fazla elektron alt kabuğu veya alt seviyesi vardır. Bu alt seviyeler, aynı açısal momentum kuantum sayısına sahip iki veya daha fazla orbital içerir l. Elektron kabukları bir atomun elektron konfigürasyonunu oluşturur. Bir kabukta bulunabilecek elektron sayısı 2 n 2'ye eşittir {\displaystyle 2n^{2}} 
Elektron kabuklarının adı, elektron gruplarının çekirdeğin etrafında belirli mesafelerde dolaştığına ve böylece yörüngelerinin "kabuklar" oluşturduğuna inanılan Bohr modelinden gelmektedir. Bu terim Danimarkalı doktor Niels Henrik David Bohr tarafından ortaya atılmıştır.