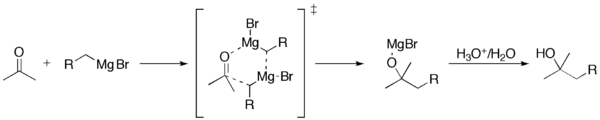
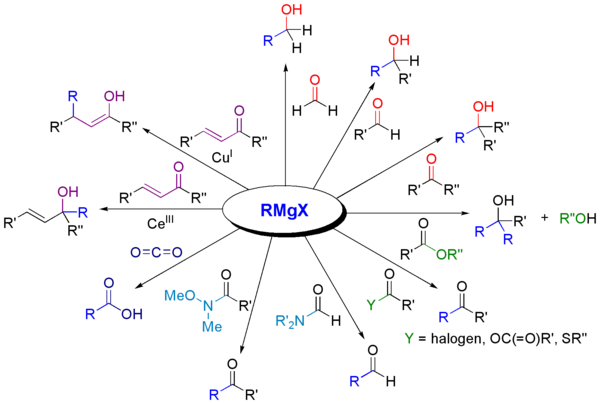
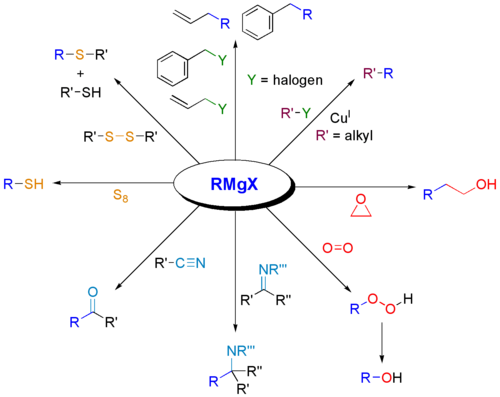
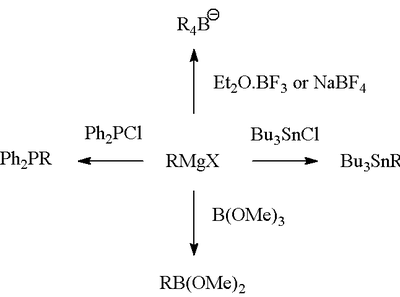
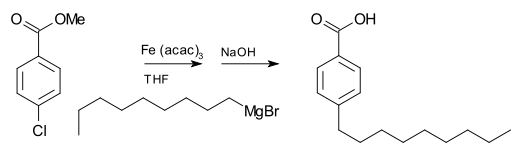
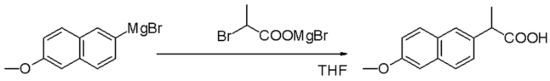
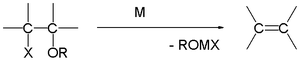
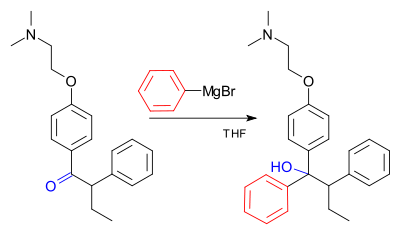
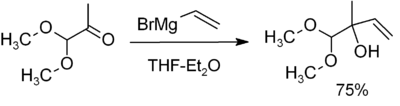Grignard reaksiyonu (/ɡriɲar/ olarak telaffuz edilir), alkil veya aril magnezyum halojenürlerin (Grignard reaktifleri) polar bağlar içinde bulunan elektrofilik karbon atomlarına (örneğin, aşağıda gösterilen örnekte olduğu gibi bir karbonil grubunda) saldırdığı organometalik bir kimyasal reaksiyondur. Grignard reaktifleri nükleofil olarak hareket eder. Grignard reaksiyonu bir karbon-karbon bağı üretir. Reaksiyon merkezi ile ilgili hibridizasyonu değiştirir. Grignard reaksiyonu karbon-karbon bağlarının oluşumunda önemli bir araçtır. Ayrıca karbon-fosfor, karbon-kalay, karbon-silikon, karbon-bor ve diğer karbon-heteroatom bağlarını da oluşturabilir.
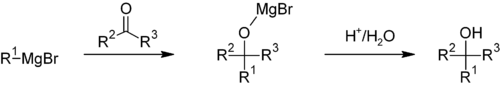
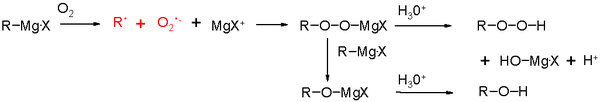
Bu bir nükleofilik organometalik katılma reaksiyonudur. Alkil bileşeninin yüksek pKa değeri (pKa = ~45) reaksiyonu tersinmez hale getirir. Grignard reaksiyonları iyonik değildir. Grignard reaktifi organometalik bir küme olarak bulunur (eter içinde).
Grignard reaktiflerinin dezavantajı, protik çözücülerle (su gibi) veya alkoller ve aminler gibi asidik protonlara sahip fonksiyonel gruplarla kolayca reaksiyona girmeleridir. Atmosferik nem, magnezyum dönüşümü ve bir alkil halojenürden bir Grignard reaktifi yapma verimini değiştirebilir. Reaksiyon atmosferinden suyu uzaklaştırmak için kullanılan birçok yöntemden biri, tüm nemi buharlaştırmak için reaksiyon kabını alevle kurutmak ve ardından nemin geri gelmesini önlemek için kabı kapatmaktır. Kimyagerler daha sonra magnezyum yüzeyini aktive etmek için ultrason kullanır, böylece mevcut suyu tüketir. Bu, Grignard reaktiflerinin mevcut suya karşı daha az hassasiyetle oluşmasını sağlayabilir.
Grignard reaktiflerinin bir diğer dezavantajı, alkil halojenürlerle SN 2 mekanizması ile reaksiyona girerek karbon-karbon bağlarını kolayca oluşturmamalarıdır.
François Auguste Victor Grignard, Grignard reaksiyonlarını ve reaktiflerini keşfetti. Bu çalışmalarından dolayı 1912 Nobel Kimya Ödülü'ne layık görülen bu Fransız kimyagerin (Nancy Üniversitesi, Fransa) adını almışlardır.