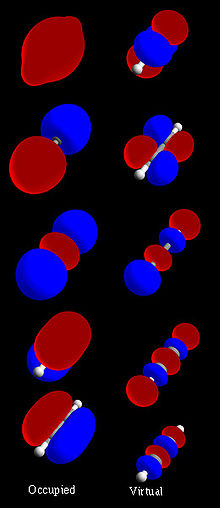
Kimyacıların moleküler yapıyı tartışabilmeleri için MO'ların geometrisini anlamaları gerekir. LCMO (Linear combination of atomic orbitals molecular orbital) yöntemi MO'ların kaba ama iyi bir tanımını verir. Bu yöntemde moleküler orbitaller, moleküldeki her bir atomun tüm atomik orbitallerinin doğrusal kombinasyonları olarak ifade edilir.
Atomik orbitallerin doğrusal kombinasyonları (LCAO)
Moleküler orbitaller ilk olarak Friedrich Hund ve Robert S. Mulliken tarafından 1927 ve 1928 yıllarında tanıtılmıştır.
Atomik orbitallerin doğrusal kombinasyonu veya moleküler orbitaller için "LCAO" yaklaşımı 1929 yılında Sir John Lennard-Jones tarafından tanıtılmıştır. Çığır açan makalesi, flor ve oksijen moleküllerinin elektronik yapısının kuantum prensiplerinden nasıl türetileceğini gösterdi. Moleküler orbital teorisine yönelik bu nitel yaklaşım, modern kuantum kimyasının başlangıcının bir parçasıdır.
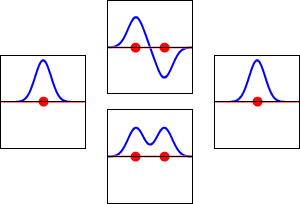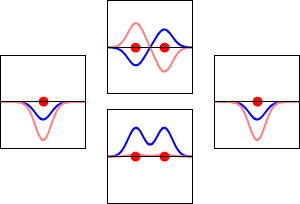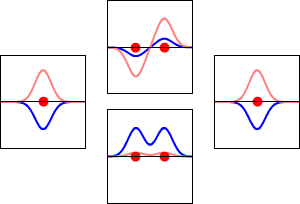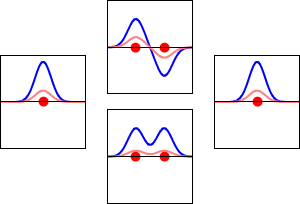
Atomik orbitallerin doğrusal kombinasyonları (LCAO), molekülün atomları birbirine bağlandığında oluşan moleküler orbitalleri tahmin etmek için kullanılabilir. Bir atomik orbitalde olduğu gibi, bir moleküler orbital için de bir elektronun davranışını tanımlayan bir Schrödinger denklemi oluşturulabilir. Atomik orbitallerin doğrusal kombinasyonları (atomik dalga fonksiyonlarının toplamları ve farkları) moleküler Schrödinger denklemlerine yaklaşık çözümler sağlar. Basit iki atomlu moleküller için, elde ettiğiniz dalga fonksiyonları matematiksel olarak şu denklemlerle temsil edilir
Ψ = ca ψa + cb ψ b
ve
Ψ* = ca ψa - cb ψ b
Burada Ψ ve Ψ* sırasıyla bağ ve karşıt bağ moleküler orbitalleri için moleküler dalga fonksiyonları, ψa ve ψb sırasıyla a ve b atomlarından gelen atomik dalga fonksiyonları ve ca ve cb ayarlanabilir katsayılardır. Bu katsayılar, tek tek atomik orbitallerin enerjilerine ve simetrilerine bağlı olarak pozitif veya negatif olabilir. İki atom birbirine yaklaştıkça, atomik orbitalleri yüksek elektron yoğunluğu alanları üretmek için üst üste biner. Böylece iki atom arasında moleküler orbitaller oluşur. Atomlar, pozitif yüklü çekirdekler ve bağlayıcı moleküler orbitalleri işgal eden negatif yüklü elektronlar arasındaki elektrostatik çekim ile bir arada tutulur.
Bağlanma, Antibağlanma ve Bağlanmama MO'ları
Atomik orbitaller etkileşime girdiğinde, ortaya çıkan moleküler orbital üç tipte olabilir: bağlanma, karşıt bağlanma veya bağlanmama.
Bağ kurma yöntemleri:
- Atomik orbitaller arasındaki bağ etkileşimleri yapıcı (faz içi) etkileşimlerdir.
- Bağ MO'ları, onları üretmek için birleşen atomik orbitallerden daha düşük enerjilidir.
Antibonding MO'lar:
- Atomik orbitaller arasındaki karşıt bağ etkileşimleri yıkıcı (faz dışı) etkileşimlerdir.
- Antibonding MO'ların enerjisi, onları üretmek için birleşen atomik orbitallerden daha yüksektir.
Bağlayıcı olmayan MO'lar:
- Bağ yapmayan MO'lar, uyumlu simetrilerin olmaması nedeniyle atomik orbitaller arasında etkileşim olmamasının sonucudur.
- Bağ yapmayan MO'lar, moleküldeki atomlardan birinin atomik orbitalleri ile aynı enerjiye sahip olacaktır.
HOMO ve LUMO
Her moleküler orbitalin kendi enerji seviyesi vardır. Kimyacılar MO'ları enerji seviyelerine göre sıralarlar. Kimyacılar elektronların önce en düşük enerji seviyesindeki MO'ları dolduracağını varsayarlar. Örneğin, bir molekülün 15 orbitali dolduracak elektronu varsa, en düşük enerji seviyesine sahip 15 MO doldurulacaktır. Listedeki 15. MO "en yüksek dolu moleküler orbital" (HOMO) ve listedeki 16. MO "en düşük boş moleküler orbital" (LUMO) olarak adlandırılır. HOMO'nun enerji seviyesi ile LUMO'nun enerji seviyesi arasındaki farka bant aralığı denir. Bant aralığı bazen molekülün uyarılabilirliğinin bir ölçüsü olarak kullanılabilir: enerji ne kadar küçükse, o kadar kolay uyarılır. Elektron uyarıldığında, boş bir MO'ya atlayacaktır. Örneğin, bu bir şeyin ışık verip vermeyeceğini (lüminesans) tahmin etmeye yardımcı olabilir.